-
일본, 제약 대국으로 재도약할 수 있을 것인가?
- 트렌드
- 일본
- 도쿄무역관 조은지
- 2024-07-12
- 출처 : KOTRA
-
일본 제약산업 부흥을 위한 일본 정부의 총력 지원 본격화
국내외 제약사∙벤처∙학계를 유치한 개방형 혁신과 CDMO 설비 정비
30년간 내리막길을 걸은 일본 의약품 시장
일본은 한때 세계 의약품 시장에서 약 20%의 점유율을 차지하던 제약 대국이었다. 그러나 1990년대 후반부터 바이오 의약품 시장으로의 전환 지연, 해외 기업과의 연구·개발 투자 규모 격차, 엄격한 규제 등으로 경쟁력이 저하됐다. 일본 국립암연구센터가 인용한 자료에 따르면, 1991년에는 글로벌 매출 상위 300개 제품 중 53개가 일본에서 개발됐으나, 2021년에는 그 수가 절반 이하로 감소했다.
<글로벌 매출 상위 300개 의약품 중 일본제약기업의 품목 수>
(단위: 개)
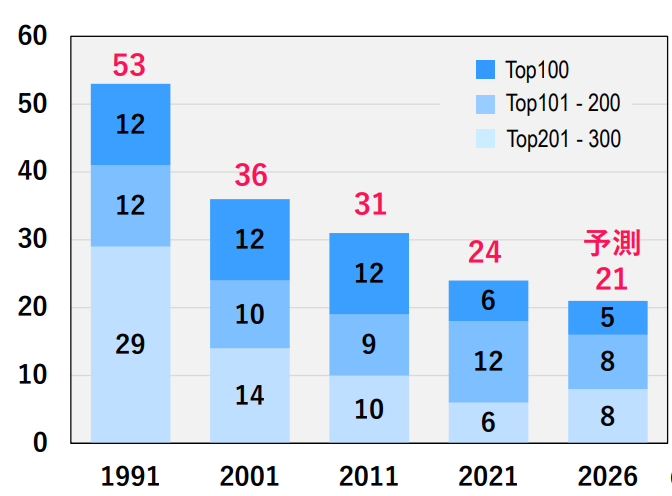
[자료: Evaluate pharma, 국립암연구센터]
글로벌 컨설팅업체 IQVIA에 따르면 세계 의약품 시장은 2022년에 1조4823억 달러(약 200조 엔)에 달할 것으로 보이며, 향후 5년간 연평균 3~6%의 높은 성장률이 예상된다. 반면 일본 의약품 시장은 같은 기간 동안 연평균 성장률이 0.3%에 불과할 것으로 전망된다. 이런 전망의 배경에는 사회보장비 예산 규모를 억제하기 위한 정부의 약가 개정이 있다. 정부의 약가 개정으로 혁신 의약품 도입이 제한되고 있기 때문이다. 최근 5년간 서구에서 승인된 신약 243개 중 일본에서 미승인된 품목이 176개에 이르며, 이 비율은 계속 상승 중이다. 글로벌 제약회사에서는 약가가 떨어지는 일본 시장에 신약을 도입하려는 유인이 저하되고 있다.
일본 정부의 약가 인하 정책으로 인해 일본 의약품 시장의 수익성이 크게 감소했다. 이로 인해 일본 내 대형 제약사들은 글로벌 M&A를 추진하며 해외로 확장하고 있으며, 세계적인 제약 회사들도 일본 내 연구소를 다른 국가로 이전하기 시작했다. 이 정책은 신약 특허 기간에도 약가를 인하하는 방침에 따른 것으로, 일본 제약 산업에 막대한 경제적 비용을 초래했다.
일본 제약공업협회의 오사카 회장은 경제산업성과의 인터뷰에서 "일본에서 신약 개발(창약, 創藥)의 공동화 현상이 일어나고 있다"라며 위기감을 표명했다. 2019년부터 전 세계를 강타한 신형 코로나 바이러스로 인해 일본은 백신을 전량 해외에서 조달해야 했다. 이로 인해 일본 정부는 유사시를 위해 필요한 기능을 국내에서 구축하는 것이 안보상 중요하다는 인식을 갖게 됐다.
일본 정부, 신약 개발 경쟁력 향상을 위한 중간 계획 발표일본 정부는 2024년 5월 22일 세계 최고의 의약품 개발 국가로서의 위치를 확립하고 의약품 산업을 주요 산업으로 육성하겠다는 기본 방향을 설정했다. 이 구상에는 신규 모달리티(Modality, 약물이 약효를 나타내는 방식)를 포함한 의약품 개발 능력 강화와 해외 의약품의 시장 진입 장벽 해소를 포함하는 종합적인 전략이 포함돼 있다. 전략의 핵심 목표는 ①최신 의약품의 신속한 제공, ②연구 강화 및 인재 유치, 그리고 ③투자와 혁신을 촉진할 인재 육성과 연구개발 환경 정비다.
일본은 신속한 신약 개발을 위해 국내외 주요 업체들과의 협력과 신규 모달리티 제조 체계 구축을 추진하고 있다. 이를 위해 다양한 인재와 글로벌 기업을 유치하고, 외국계 제약기업 및 벤처캐피탈이 참여하는 관민 협의회를 설치해 '신약개발(창약) 에코시스템'을 실현하려 한다. 이 구상은 외국계 제약기업의 수요를 바탕으로 해외 기업과 자본을 일본으로 유치하려는 목적이다.
<「신약개발력 향상으로 국민에게 최신 의약품을 신속하게 제공하기 위한 구상회의」 중간 보고서>일본의 신약 개발력 강화
-외국제 제약사와 VC도 포함하는 관민 협의회 설치
-국제 수준의 임상시험 체제 정비 및 국제 협력 추진
-신규 모달리티 의약품의 국내 제조 체제
* CDMO 지원강화, 국제 수준의 CDMO와 FIH 시험 실시 거점의 융합 및 해외거점과의 제휴
-국내외 학계-스타트업-제약기업-VC 매칭 통한 창약 시즈 창출
최신 의약품 신속한 제공
-약사규제의 재검토 및 운용 개선
-소아 난치병 희소 질병 의약품의 개발 촉진
-PMDA의 상담 / 심사 체제
투자와 혁신 선순환 구축
-혁신의약품의 가치에 따른 평가
-바이오시밀러 사용 촉진
-스위치 OTC화 추진 등에 의한 셀프케어와 셀프 메디케이션 추진
[자료 : 내각관방(2024.5.22.)]
이외에도 일본은 스타트업 지원을 강화하고 희소 의약품 확보를 위한 약사 규제 완화, 국제 공동 임상실험 추진을 포함한 새로운 정책을 발표했다. 또한 바이오 분야 인재 육성과 해외 플레이어 초청, 의약품 개발 및 제조 수탁(CDMO) 지원 강화책도 제창됐다. 이러한 조치들은 일본의 의약품 산업 경쟁력 강화를 목표로 하고 있다.
일본의 백신 국내 생산설비 정비 및 임상시험 지원 확대
일본 정부는 2021년부터 유사시에 백신 생산 가능한 체계를 정비하기 위해 '백신 생산 체제 강화를 위한 바이오의약품 제조 거점 등 정비사업'을 추진하고 있다. 이 사업은 일본 국내에서 GMP 레벨의 백신 및 바이오 의약품을 생산할 수 있도록 설비를 정비하고 백신 부품 소재의 국산화를 추진한다. 평시에는 항체의약품과 원약을 생산하고, 유사시에는 감염증 백신 생산으로 전환할 수 있는 듀얼유즈(Dual Use) 설비를 도입해 국내 백신 조달 체계를 구축하는 것이 목표다.
일본은 백신 제조 인프라 강화를 위해 두 차례에 걸친 공모를 통해 프로젝트를 선정했다. 2021년 첫 공모에서는 17개 프로젝트가 선정돼 보정 예산 2265억 엔이 할당됐으며, 2022년 두 번째 공모에서는 23개 프로젝트가 선정돼 955억 엔 규모의 자금이 지원됐다. 첫 번째 사업자는 2027년까지, 두 번째 채택자는 2028년까지 백신 생산 체계 구축을 완료할 계획이다.
<백신제조거점 정비사업 공모 채택자 현황①>구분
기업(소재지)
유사시 제조백신
백신제조거점
정비사업
ARCALIS(후쿠시마)
mRNA
다이이치산쿄(사이타마)
mRNA
AGC(가나가와)
mRNA, 바이러스벡터, 재조합, 유전자개변세포
모더나재팬(가나가와)
mRNA
후지필름후지화학(후쿠야마)
mRNA, 바이러스벡터, 재조합
타카라바이오(시가)
mRNA, 바이러스벡터
JCR파마(효고)
바이러스벡터, 재조합, 불활화
KM바이오로직스(쿠마모토)
바이러스벡터, 재조합, 불활화, 약독화 생백신
제제화
충전거점
정비사업메이지세이카파마(가나가와)
mRNA
니프로파마(시가)
mRNA, DNA, 바이러스벡터, 재조합, 신규 모달리티
시오노기파마(오사카)
mRNA, DNA, 바이러스벡터, 재조합, 불활화, 약독화 생백신, VLP
부슈제약(사이타마)
바이러스벡터, 재조합단백질, 불활화, VNP, DNA
임상시험약
제조거점ELIXIRGEN SCIENTIFIC JAPAN(가나가와)
mRNA
오사카대학 미생물병연구회(카가와)
바이러스벡터, 재조합, 불활화, 약독화 생백신, 핵산
히로시마대학(히로시마)
mRNA, DNA, 펩틴
VLP테라퓨틱스재팬(후쿠오카)
바이러스벡터, 재조합단백질, VNP, DNA, 자기증식 RNA
[자료: 경제산업성]
<백신제조거점 정비사업 공모 채택자 현황②>
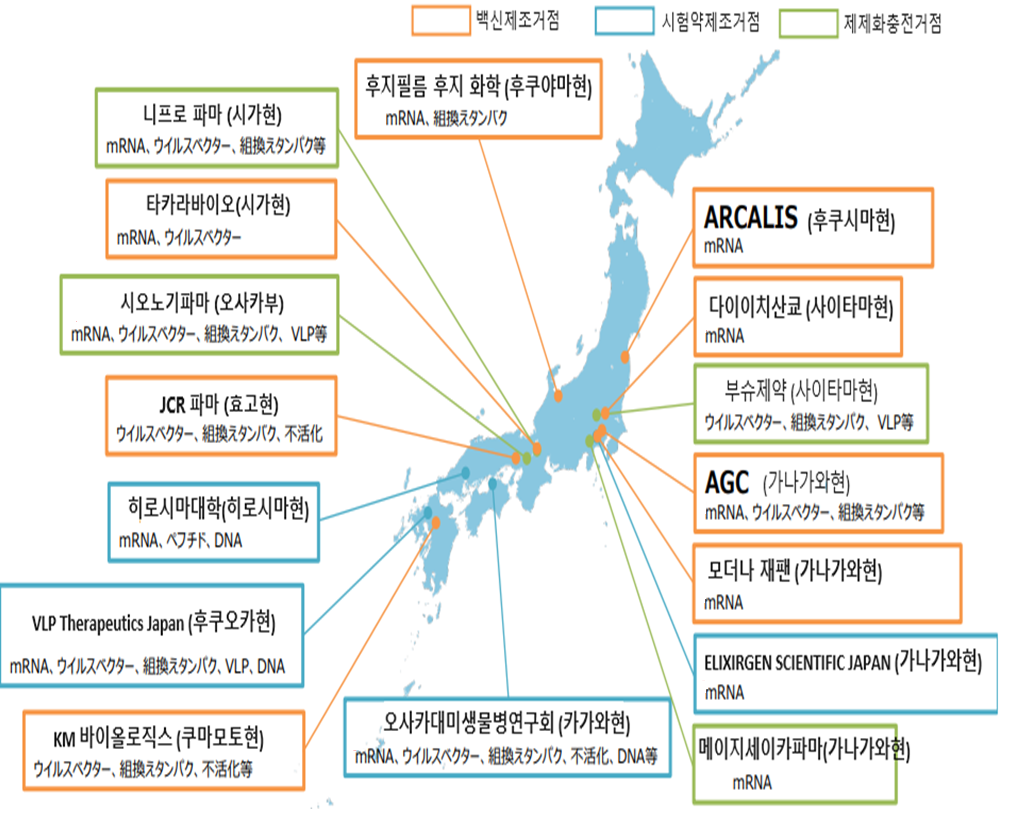
[자료: 경제산업성]
백신 국산화를 추진하려는 일본 정부의 노력은 2003년에도 시도된 바 있었는데, 당시에는 백신 국산화의 중요성과 일본의 생산 기반 취약성에 대한 논의가 이루어졌다. 그러나 당시 연구개발 비용 회수에 대한 불확실성과 백신 임상 실험 경험 부족이 발목을 잡았다.
2024년 2월 후생노동성은 2024년 2월 '백신 대규모 임상시험 등 사업'에 대한 공모를 진행했으며, 6월 18일에 다이이치 산쿄와 KM 바이오로직스의 프로젝트를 선정했다고 발표했다. 이 사업을 통해 국내 제약 기업들이 백신 개발에 도전할 수 있도록 지원하는 것을 목표로 하고 있다.
‘백신 대규모 임상시험 등 사업’은 대규모 임상시험을 통해 백신의 유효성을 검증하고, 경험과 지식을 축적해 차기 팬데믹 대비 백신의 신속한 개발을 목표로 한다. 일본 내에서 실시될 이 프로젝트는 1상, 2상 임상시험에서 백신의 유효성과 안전성을 확인한 후, 국제 공동으로 실증적인 임상시험을 진행한다. 각 사업에는 최대 500억 엔의 조성금이 배정된다.한국의 최근 대일본 의약품 수출 동향
최근 미용 의료기기를 중심으로 한국의 일본으로 의료기기 수출이 호조를 보이는 것과 달리, 의약품 수출은 다소 주춤한 모습을 보이고 있다.
한국의 대일본 의약품(MTI코드 2262) 수출액은 2024년 5월까지 누계 기준 2억9850만 달러로 전년 동기 대비 △25.3% 감소하며 2023년 하반기 이후 부진한 추세를 보인다. 특히 한국의 대표 의약품 수출 품목인 바이오 원료 의약품(HS코드 3002.14)의 대일본 수출 증감률은 같은 기간 △68.5%로 상당히 저조하다.
이런 부진의 배경에는 일본의 불안정한 의약품 수입 수요가 존재한다. 일본의 2024년 5월까지 누계 기준 대세계 의약품 수입액(HS코드 3002, 3004, 3006 합계)은 전년 동기 대비 △9.3% 감소했고, 가장 큰 수입 대상국인 미국으로부터의 수입도 같은 기간 △19.0% 감소했다. 특히 일본에서는 2021년 이후 대형 제네릭 제약사 13개사가 품질 부정으로 행정처분을 받았는데, 행정처분으로 인한 출하 중단으로 원료의약품 시장이 불안정한 상황이다. 예컨대 2021년 업무 정지가 내려진 제네릭 제약사 니치이코는 총 574개 품목의 판매를 중지했으며, 이 중 36개 품목*은 한국 제조사의 원료의약품(API)이 등재된 품목이었다. (*출처: 제5회 한일 의약품 공동 심포지엄, 2023.9.)시사점
일본 정부는 신약 및 백신 개발 경쟁력 향상을 위해 민관 합동으로 적극적인 자금 투자, 벤처 육성, 국내외 주요 업체들과 협력을 추진하고 있다. 또한 IQVIA에 따르면, 일본 의약품 시장은 타 지역 대비 상대적으로 낮은 연평균 성장률에도 2028년 여전히 세계 3위 규모를 유지할 것으로 전망된다. 우리 제약·바이오 기업들이 여전히 일본 의약품 시장에 주목해야 하는 이유다.
일본 의약품 시장 진출을 위해서는 철저한 사전 준비와 인증 취득이 필요하다. 일본은 안전성, 효과성, 품질을 중시해 검증되지 않은 성분에 대해 엄격한 규제를 적용하고 있다. 의약품 수출을 고려할 때, 제품 성분이 일본 규제를 충족하는지 철저히 검토하는 것이 중요하다. 이 과정에서 일본 PMDA(Pharmaceuticals and Medical Devices Agency)나 관련 규제 기관의 최신 규정 확인과 전문가의 조언이 필요하다.
헬스케어 유통 대기업 A사 신사업부의 간부는 "일본 의료용 의약품 시장은 거의 쇄국 상황이라고 봐도 좋을 정도로 수입이 까다롭고 일부의 전문 수입 상사를 통해서만 가능하기 때문에 시장 진입이 쉽지 않다"라며 국내기업 일본 수출 시에는 노하우를 보유한 수입 밴더와 매칭이 되는 것이 중요하다는 점을 밝혔다. 아울러 "최근 고령화 현상 대응 및 수명 연장을 위한 서플리먼트, 건강식품, 헬스케어 상품은 해외에서도 조달을 하기 위해서 꾸준히 탐색을 늘리고 있다"라며 한국 헬스케어 관련 의약품에 대한 관심을 표명했다.
또, 의약품 수출에는 중간 유통사나 제약회사와의 파트너십이 중요하며, CPHI Japan, Interphex Japan과 같은 현지 전시회, 매년 10월 국내에서 개최되는 KOTRA 글로벌바이오파마 플라자(GBPP) 수출 상담회 참가를 통해 네트워크 구축이 가능하다. 글로벌바이오파마 플라자(GBPP)는 무역투자24 홈페이지를 통해 참가 신청이 가능하니 참고바란다.
<일본 의약품 전시회 정보>
전시회명
제26회 Interphex Japan
개최시기/회장
2025.7.9.(수) ~ 7.11.(금) / 도쿄 빅사이트
동시 개최전
① 인터펙스재팬(의약품 화장품 제조전)
② 인파마재팬(의약품원료전)
③ 바이오의약엑스포
④ 파마랩 EXPO 도쿄(의약품연구개발전)
⑤ 재생의료 EXPO 5개의 전시회를 동시에 개최
출전 규모
출전사 838개사, 방문객 3만2000명 (24년 기준)
전시회명
제22회 CPHI Japan(국제의약품개발전)
동시개최
파마IT & 디지털 헬스 엑스포, Medtec(의료기기전)
개최시기/회장
‘25. 4.9.(수) ∼ 11(금), 10:00∼17:00 / 도쿄 빅사이트(4~6홀)
출전 규모
출전사 650개사, 방문객 2만5000명(24년 기준)
자료: Evaluate pharma, 국립암연구센터, 내각관방, 경제산업성, KOTRA 도쿄 무역관 자료 종합
<저작권자 : ⓒ KOTRA & KOTRA 해외시장뉴스>

KOTRA의 저작물인 (일본, 제약 대국으로 재도약할 수 있을 것인가?)의 경우 ‘공공누리 제4 유형: 출처표시+상업적 이용금지+변경금지’ 조건에 따라 이용할 수 있습니다. 다만, 사진, 이미지의 경우 제3자에게 저작권이 있으므로 사용할 수 없습니다.
-
1
2021년 일본 의료기기 산업 정보
일본 2022-01-20
-
2
2024 통상백서로 살펴보는 일본 통상정책과 과제
일본 2024-08-22
-
3
장기화되고 있는 일본 의약품 부족 사태
일본 2024-05-31
-
4
AI4BELGIUM 전략에 따라 발전하고 있는 벨기에 AI 생태계
벨기에 2024-09-04
-
5
일본 의약품 시장동향
일본 2024-08-13
-
6
일본 의약품 시장 동향
일본 2022-10-21
-
1
2021년 일본 석유산업 정보
일본 2022-01-20
-
2
2021년 일본 의료기기 산업 정보
일본 2022-01-20
-
3
2021년 일본의 산업 개관
일본 2021-12-29
-
4
2021 일본의 정보 보안 산업
일본 2021-12-29
-
5
2021 일본의 수산업
일본 2021-12-29
-
6
2021 일본의 자동차 산업
일본 2021-12-29













