-
[기고] 인도네시아 의료기기 및 생활가정용품의 보건부 등록 관련 참고사항 안내
- 외부전문가 기고
- 인도네시아
- 자카르타무역관 박승석
- 2022-01-07
- 출처 : KOTRA
-
건강에 영향을 미칠 수 있는 의료기기와 중요 생활가정용품 수입을 위해서는 인도네시아 보건부 등록이 필요
의료기기는 ALKES, 중요 생활가정용품은 PKRT라 하며, 의료기기 유통허가(IPAK)을 가진 현지 법인이 진행해야 함
신속한 보건부 등록을 위해 사전에 현지에서 요구하는 자료에 대한 철저한 대비가 필요
임준환(jhlim9971@hanmail.net) PT. Green Nature Farm / CEO
서론
인도네시아 정부의 지난 2014년 건강보험제도인 BPJS(Badan Penyelenggara Sosial Kesehatan) 도입 이후 의료 서비스에 대한 일반 국민들의 접근성이 증가했다. KOTRA 자카르타무역관 의료기기 시장 조사에 의하면 세계 4위인 인구 대국인 인도네시아의 의료 산업은 소득 수준의 향상과 의료 체계 정비에 따라 지속적으로 성장하고 있다. 더해서 코로나 19를 겪으며 건강에 대한 관심이 높아지면서 앞으로의 성장 전망도 밝은 편이다. 이에 따라 우리 의료기기 기업들의 인도네시아 시장 진출 문의도 증가하고 있어 이번 기고에서는 인니 의료기기 시장 진출을 위한 제품에 등록 허가를 관할하는 인도네시아 보건부(Depkes)의 등록 준비와 절차 그리고 주요 업무 사항에 대하여 소개를 하고자 한다. 인도네시아 의료기기의 시장 동향 및 현황은 코트라의 시장 현황 보고서와 보건산업진흥회 등 관련 유관기관의 조사 보고서를 참조 활용하기를 바란다.
본론 1 : 인도네시아 보건부 업무 소개 – 제품별 등록 유형
보건부(MOH-Depkes)는 의료기기(Medical Device)와, 의료기기는 아니지만 건강에 영향을 미칠 수 있는 중요 생활가정용품(Household)의 인허가도 담당하고 있다. 여기서 인허가란 제품의 생산부터 유통에 대한 전반적인 관리와 감독을 의미한다. 의료기기 등록은 ALKES(Alat Kesehatan)라고 하며, 생활가정용품 등록은 PKRT(Perbekalan Kesehatan Rumah Tangga)라고 한다. 수입제품 의료기기 등록을 위해서는 두 가지 방법이 있다. 먼저 인도네시아 현지 수입회사에 위임을 통해 등록 진행을 할 수 있다. 등록을 위임 받은 현지 수입회사는 의료기기 수입 유통 허가인 IPAK(IZIN Penyalur alat kesehatan) 면허를 필수적으로 보유해야 제품 등록 신청이 가능하다. 그 다음으로는 직접 현지 투자 법인을 세워 IPAK 허가를 받은 뒤 제품의 보건부 등록을 진행하는 것이다.
ALKES 등록의 경우는 위 설명과 같이 IPAK이라는 수입 유통 면허를 보유한 기업만 가능하며, PKRT 등록은 IPAK 보유가 의무사항은 아니며, 사업 영업 사항에 중요가정생활용품의 분야가 포함되어 있으면 등록이 가능하다. 필자는 우선 한국과 다른 분류 체계를 적용 받고 있는 중요가정생활용품과 한국과 비슷한 등급 체계인 의료기기의 분류 유형에 대하여 소개하고자 한다.
1) 중요가정생활용품(Household)
한국에서는 공산품 등으로 특별한 사전 허가가 요구되지 않는 분야일 수 있으나 인니 규정상 모기향, 모기 스프레이, 모기 기피제, 유아용 젖병, 자동차 방향제, 식기 세제, 세탁 세제, 소독제, 비누, 물 티슈, 화장지 등이 해당 된다. 미용과 관련한 품목, 예를 들면 화장비누, 화장용 물티슈와 같은 제품은 식약청(BPOM)의 허가가 필요하다. 중요가정생활용품을 PKRT(Perbekalan Kesehatan Rumah Tangga)로 표기하며, 등급은 Class 1 ~ Class 3으로 구분한다. 보건부 심사 등록 납입 비용은 1백만 루피아(Class 1), 2백만 루피아(Class 2), 3백만 루피아(Class 3)다. Class의 구분은 위험도에 따라 구분되며 Class 3이 가장 높은 위험도 등급이다. 해당 구분은 한국의 분류 체계와 상이해 수출을 진행하게 되는 경우 현지 수입 위임사와 협의해 유사 제품의 등록 사례나 보건부 웹사이트의 분류 기준(http://regalkes.kemkes.go.id/#home/informasi/lstGuideline)을 조회할 필요가 있다. 2021년 12월 기준, 월 평균 400~600건의 PKRT 제품이 신규로 보건부 인허가를 통과하고 있으며, 수입 제품 등록은 약 30%정도 비중을 차지하고 있다.
<PKRT 품목 인도네시아 보건부 등록 현황(12.27 기준)>
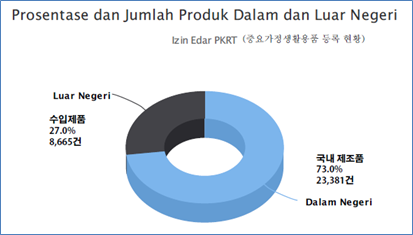
[자료: 인도네시아 보건부]
2) 의료기기(Medical Device)
한국의 의료기기 분류 등급 체계와 유사하다. 의료기기의 등록 및 신청을 위해서는 인도네시아 수입사가 필수 위임사가 되어야 하며 같은 제품명에 대하여 중복 등록이 불가해 특히 주의가 요구된다. 더해서, 위에 설명한대로 수입사는 IPAK 면허를 필수적으로 보유해야 한다. 인도네시아 의료기기의 등급은 Class 1/A, 2a/B, 2b/C, 3/D등급과 같이 A,B,C,D 4개 등급으로 구분하며, 구분 기준은 제품의 위험도 정도이다. 보다 자세한 사항은 아래와 같다.
<위험도에 따른 의료기기 구분>
등급
의료기기 구분
심사 등록비
Class 1/A
오용을 하더라도 환자에 유의미한 결과를 야기하지 않는 의료기기
1,500,000
Class 2a/B
오용하면 환자에게 유의미한 결과를 초래할 수 있지만 치명적이지 않은 의료기기
3,000,000
Class 2b/C
환자 건강에 영향을 미칠 수 있어 의료기기 등록 시 위험 평가서와 안전성을 입증하는 평가 결과를 제출해야 함
3,000,000
Class 3/D
환자, 간호사 등 관련자에게 치명적인 결과를 초래할 수 있는 제품으로 유통 전 제품등록 과정에서 반드시 위험 평가서와 안전성을 입증하는 평가 결과, 임상시험 결과 등을 제출해야 함
5,000,000
[자료: 인도네시아 보건부(http://regalkes.kemkes.go.id/#home/informasi/lstGuideline)]
인도네시아 의료기기 등록 현황을 보면, 수입에 대한 의존도가 매우 높은 편이다. 이에 따라 정부에서는 의료기기 TKDN 정책 수립을 포함해 의료기기 수입 대체를 위해 다양한 정책을 추진하고 있다. 이와 같은 정책 기조는 코로나19로 인해 의료기기 수입이 증가하자 더욱더 강화되고 있는 추세로 보인다.
<ALKES 품목 인도네시아 보건부 등록 현황(12.27 기준)>
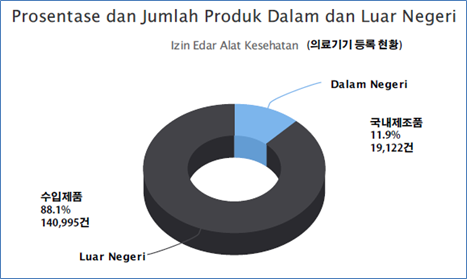
[자료: 인도네시아 보건부]
3) 제품의 등록 신청 서류 안내
먼저, 신청에 대해 말하자면 ALKES와 PKRT 신청은 온라인으로 이루어진다. 인도네시아 보건부 사이트(http://regalkes.kemkes.go.id/)에서 신청 가능하다.
그 다음으로 준비해야할 서류를 살펴보겠다. 공통적으로는 위임장인 LOA(Letter of Authorization)와 자유판매증명서인 CFS(Certificate of free sales) 준비가 필요하다. 먼저 LOA를 보면 최소 위임 기간을 2년 이상 설정해야 하며, 주한 인도네시아 대사관 영사과(여의도 소재)의 최종 공증이 필요하다. CFS는 한국 식품의약품안전처가 발급하고 있으며, 국내외 판매용이라는 문구가 필수적으로 들어가야 한다. 공증 대상은 아니고, 보건부 플랫폼에 전자문서 형태로 제출한다. 다만, 의료기기가 아닌 공산품은 한국화학시험연구원, 섬유시험연구원, 환경산업기술원과 같은 국가 연구원에서 품목별로 담당하고 있다.
이 밖에도 ISO 인증과 시험성적서 등 각종 서류 준비가 필요하다. 해당 서류는 ALKES와 PKRT에 따라 조금씩 다르다. 먼저 PKRT를 등록하는 경우 ISO 9001 인증과 제품의 기술/품질/안전성 관련한 자료 및 포장 디자인 전개도/시험성적서 등이 필요하다.
ALKES를 등록하는 경우 ISO 13485나 의료기기 제조사 인증인 Medical Device GMP(Good Manufacturing Product), 만약 의료기기 소프트웨어의 경우에는 IEC 62304 인증이 필요하다. 더해서 제품의 기술/품질/안전성 관련한 자료와 포장 디자인 전개도/시험성적서 등도 필요하다.
본론 2 : 인도네시아 보건부(MOH) 주요 업무 가이드 및 개정법에 따른 이슈 소개
1) 주요 개정법 사항
의료기기 수입 및 유통에 관련한 외국인 지분 취득 한도 개정
대통령령 2021년 10호 제 3항에 의거해 의료기기 수입 및 유통관련 외국인 투자 지분 제한이 완화되었다. 기존에는 의료기기 수입이나 유통관련 법인을 설립하는 경우 외국인 지분 취득이 최대 49%까지만 가능했지만, 상기 법령에 의해 외국인 지분 취득이 100%까지 가능해졌다. 즉 외국 투자 법인도 의료기기 수입 및 유통관련 업무를 진행할 수 있게 되었다.
PKRT 소독제에 대한 WHO 권고 의무 시험 추가
PKRT 등록 대상인 소독제에 대한 2021년 4월 신규 조항에 따라 WHO 권고 의무 시험 검사가 추가되었다. 공기소독제품은 AOAC 961.02.2012 시험검사법이 적용된 멸균 시험 검사가 필요하다. 이 밖에 향균 및 박테리아 사멸용 소독제는 SNI EN 1276; SNI EN 13727+A2 시험 검사법, 곰팡이균 사멸용 소독제는 SNI EN 1650; EN 13624 시험 검사법 적용 결과가 필요하다.
모든 기능이나 제품에 멸균 대상의 표기를 위하여는 3가지의 시험을 모두 받아야 하며, 해당 시험검사법이 적용 된 결과서 제출이 필요하다.
코로나19 Antigen 진단기기 등록 전 지정 시험 기관을 통한 민감도 테스트 의무화
ALKES 등록이 필요한 Antigen 진단기는 등록 전에 인도네시아 보건부에서 지정한 7개 시험 기관 중 한곳에서 의무적으로 민감도 테스트를 받아야 한다. 해당 조치는 2021년 4월부터 시행 중이며 비용은 시험 기관별로 상이(USD 6,000 ~ USD 10,000)한 것으로 알려져 있다.
수입유통허가와 의료기기 제조허가에 대한 등록 플랫폼 통합
수입유통허가(IPAK) 및 의료기기 제조허가(SPAK)에 대한 신규 등록 신청과 심사를 모두 인도네시아 투자부에서 관리하고 있는 OSS(Online Single Submission)로 이관했다. 단 심사 평가와 허가는 보건부에서 관리하고 있다.
2021년 7월 29일자로 기존 등록 사이트에서 신규 접수가 불가하다. 다만 시스템 최적화 문제로 일부 애로사항이 있는 것으로 알려져 있다. OSS 시스템에서 등록을 진행하면 기존 보건부 심사 시스템과 연동에 문제가 있어 접수와 심사가 매끄럽지 못하다. 해당 문제에 대해 문의해보니 OSS시스템 관리팀과 보건부에서는 조속히 정상화 하겠다는 답변만 있으며 언제 정상화 될지는 명확하게 답하지 않은 상황이라, 지속적인 상황 파악이 필요하다.
2) 실무 참고사항
IPAK 및 SPAK의 신청 조건을 충족하기 위해서는 책임 관리인(PJT, Penanggung Jawab Teknis)을 정식 근로자로 채용해야 한다. 책임 관리인은 화학, 생물학, 약학, 의학 전공자로 4년제 이상 학력이 요구 된다. 취급하는 제품의 유형에 따라 IPAK과 SPAK에서는 카테고리 신청이 구분되며 진단 및 시약, 전자기 방사선, 전자 의료 비방사선 등 5가지 구분이 있다.
3ply 마스크와 같이 비의료기(Non-Medical) 제품을 신고하는 경우 외관 외형상 수술용 마스크(Surgical Mask)와 구분이 어려워 의료기기용이 아닌 일반 마스크의 경우 세관 통과를 위해 'Medical grade' 또는 'Sugical mask'라는 표현과 표기를 하지 말아야 한다. 또한 가급적 비의료기기 신고인 SKP(Surat ketrangan produksi)를 보건부에 신청하여 확인서를 받아 두는게 수입과 유통 및 판매나 현지 기관의 불시 단속 대비에 용이하다. 신청 사이트는 http://esuka.binfar.kemkes.go.id/portal 이다.
의료기기 제품 별로 ALKES 신청 전에 별도에 사전 허가나 등록이 필요한 제품도 있어 사전에 확인이 꼭 필요하다. 예를 들면, 2b C 에 속하는 X-ray 장비 시스템류의 경우는 인도네시아 BAPETEN(방사능 관리청)에 별도 제품 등록 및 허가 이후 보건부에 제품 등록 신청을 진행해야 한다.
한국 제품 구분 유형에 공산품인 세제류가 인니에서는 보건부 PKRT 등록 대상이며, 한국에서 의약외품인 치약은 인도네시아 식약청(BPOM) 화장품 유형에 등록이 필요하고 칫솔은 인도네시아 기준 보건부 의료기기에 적용 되고 있어 등록을 위해서는 ISO 또는 CFS 발행이 필요하다. 이와 같이 품목별로 사전 확인을 통해 전체 일정을 계획해야 한다.
결론 및 제언
인도네시아의 보건 관련 상품의 시장은 의료기기 및 미용 의료기, 소비재 의료기기 등 그 분야와 시장 진출 품목 대상이 확대되고 있어 해외 시장 개척지로 매우 중요한 국가이다. 현재 인도네시아의 의료기기 수입에서 한국 제품 수입은 5위를 차지 하고 있고, 우리기업들의 진출이 확대되고 있는 추세다. 하지만 정부의 의료기기 국산화 정책 추진 장려 기조와 기존 의료기기 유통 기업들과의 경쟁도 심화되고 있어 면밀한 검토가 필요하다.
인도네시아의 보건부는 등록이 필요한 제품이 특수한 기능을 갖거나 사용상 주의 및 관리가 필요하다고 판단되면 많은 근거 서류와 검증을 요구 하고 있다. 현지 수입사의 자체 준비만으로 진행이 어려운 부분도 상당수 존재하고 있는 만큼 한국 수출사(제조사)도 이와 같은 현지 상황에 따라 현지 등록 기준에 부합하는 서류 준비를 포함해 파트너와 적극적으로 소통하며 협업하는 것이 필요해 보인다.
※ 이 원고는 외부 글로벌 지역전문가가 작성한 정보로 KOTRA의 공식 의견이 아님을 알려드립니다.
<저작권자 : ⓒ KOTRA & KOTRA 해외시장뉴스>

KOTRA의 저작물인 ([기고] 인도네시아 의료기기 및 생활가정용품의 보건부 등록 관련 참고사항 안내)의 경우 ‘공공누리 제4 유형: 출처표시+상업적 이용금지+변경금지’ 조건에 따라 이용할 수 있습니다. 다만, 사진, 이미지의 경우 제3자에게 저작권이 있으므로 사용할 수 없습니다.
-
1
보건의료 정책동향 및 유망분야 살펴보기, 메디컬 웨비나 개최(2편)
인도네시아 2021.10.13
-
2
의료기기 시장 진출 길라잡이, 메디컬 웨비나 개최(1편)
인도네시아 2021.10.13
-
3
인도네시아 의료기기 시장 동향
인도네시아 2020.11.30
-
4
메디컬 온라인 로드쇼 2020을 통해 살펴본 인도네시아 의료시장 현황 및 진출방안
인도네시아 2020.10.05
-
5
인구 세계 4위 인도네시아, 초음파 영상 진단기는 필수 의료 장비
인도네시아 2019.07.25
-
6
인도네시아 의료시장 진출전략 세미나 취재기
인도네시아 2018.08.23
-
1
인도네시아 의료기기 시장 동향
인도네시아 2020-11-30
-
2
의료기기 시장 진출 길라잡이, 메디컬 웨비나 개최(1편)
인도네시아 2021-10-13
-
3
미국의 차세대 전력망 ESS 도입
미국 2022-01-13
-
4
차세대 전력 반도체, 미래 전자 제품의 혁신을 주도한다
미국 2022-01-14
-
5
보건의료 정책동향 및 유망분야 살펴보기, 메디컬 웨비나 개최(2편)
인도네시아 2021-10-13
-
6
[기고] 화장품, 식음료, 건강기능식품 진출 전 필독! 식약청(BPOM) 인증 총정리
인도네시아 2021-11-24
-
1
2021년 인도네시아 소비재 산업 정보
인도네시아 2022-01-10
-
2
2021년 인도네시아 기계 산업 정보
인도네시아 2022-01-10
-
3
2021 인도네시아 건설 산업 정보
인도네시아 2022-01-07
-
4
2021년 인도네시아 섬유산업 정보
인도네시아 2022-01-07
-
5
2021년 인도네시아 석유화학산업 정보
인도네시아 2021-12-28
-
6
2021년 인도네시아 신재생에너지 산업 정보
인도네시아 2021-10-25













