-
아세안 비관세장벽 ③ - 의료기기
- 통상·규제
- 싱가포르
- 싱가포르무역관 Yi Yang
- 2016-11-23
- 출처 : KOTRA
-
[KOTRA 싱가포르 무역관에서는 11월 한 달 동안 아세안 비관세장벽 현황을 파악하고, 비관세장벽의 영향을 받는 주요 분야인 철강, 의료기기, 전기전자 분야에 대한 비관세장벽 현황 및 대응방법 소개를 위한 '아세안 비관세장벽 심층분석' 시리즈를 총 4개(현황, 철강, 의료기기, 전기전자) 게시물을 통해 연재합니다.]
□ 아세안의 의료기기 수입 현황
ㅇ 아세안 의료기기 수입 시장 동향
- 아세안 의료기기 시장은 지속적으로 확대되고 있으며, 2016년 아세안 6개국(싱가포르, 말레이시아, 태국, 인도네시아, 필리핀, 베트남)의 의료기기 시장규모는 전년보다 약 9% 증가할 것으로 예상됨.
- 아세안에서 의료기기는 대부분 수입에 의존하기 때문에, 의료기기 수입 시장도 2011년의 51억 달러에서 2015년 66억 달러에 이르러 연평균 6.8%로 성장하고 있음.
- 2015년 기준으로 아세안의 주요 의료기기 수입 대상국은 미국(25.1%), 중국(10.9%), 독일(10.0%), 일본(8.8%), 멕시코(6.7%) 순으로, 한국산은 3.0%의 시장점유율로 9위를 차지함.
ㅇ 한국의 대아세안 의료기기 수출 동향
(단위: 백만 달러, %)
2013
2014
2015
2016.1~8 누계
비중
(2016.8 기준)
아세안
217
223
239
156
100
베트남
45
50
56
43
27.5
싱가포르
54
52
52
32
20.3
태국
35
34
37
24
15.5
필리핀
15
19
23
19
12.4
인도네시아
29
24
31
14
11.7
자료원: 한국무역협회
- 아세안에서 한국의 주요 의료기기 수출 대상국은 베트남, 싱가포르, 태국, 필리핀, 인도네시아로, 5개국에 대한 수출규모는 한국의 대아세안 전체 수출규모의 84.6% 차지
□ 우리 기업의 대아세안 수출 시 주요 비관세장벽
ㅇ 아세안에 의료기기 수출할 때 복잡한 인증·등록 절차 등의 비관세장벽의 영향을 받고 있음. 서류 준비에 많은 시간과 비용이 소요되기도 하고, 베트남 등 국가는 중고 의료기기에 대한 수입금지 조치도 시행하고 있음.
ㅇ 베트남
- 베트남 정부는 국민건강과 의료안전을 위해 의료기기 수입하는데 많은 비관세장벽을 두고 있음.
- 베트남은 자국 제조업과 부품소재산업 육성을 강화하기 위해 중고품목의 수입금지를 지속적으로 확대하고 있음. 현재 의료기기 부문 베트남 수입규정에 따르면, HS Code 9018~9022에 해당하는 모든 의료기기의 중고 제품은 수입이 불가함.
- 새 의료기기 수출할 때도 법적, 인적, 품질, 시설 등 여러 조건을 만족해야 하는 복잡한 등록 절차를 통해야 함.

자료원: 한국보건산업진흥원, KOTRA 호치민 무역관 자료 종합
ㅇ 싱가포르
- 싱가포르에서 수입 의료기기에 대해 엄격한 비관세장벽을 두고 있으며, 생산, 수입, 유통하는 의료기기는 싱가포르 보건과학청(HSA)에 등록하는 것을 의무화하고 있고, 제품 등록은 매년 갱신해야 함.
- 싱가포르의 의료기기는 위험도의 낮음부터 높음의 순서로 A~D 등급으로 나뉘며, 또한 해외 인정 국가(호주, 캐나다, 일본, 미국, 유럽)에서의 제품 시판 경험에 따라 '즉시, 긴급, 축약, 전체' 4개의 트랙으로 분류해, 각 등급과 트랙에 따라 심사 소요 시간과 비용이 다름.
* 즉시(Immediate): 인정 국가 중 최소 두 군데 이상에서 허가를 받고 해당 관할지에서 최소 3년 이상 제품을 판매했으며, 최소 2년 이상 전 세계적으로 해당 제품 관련 안전 문제가 발생하지 않았고, 위 규제 기관 중 어느 한 곳에서도 제품 인증을 거부당하지 않은 경우
* 긴급(Expedited): 인정 국가 중 최소 한 곳 이상 허가받고 해당 관할지에서 최소 3년 이상 제품 판매했으며, 최소 3년 이상 전 세계적으로 안전 문제 발생하지 않은 경우, 또는 위 인정 국가 중 최소 두 군데 이상 허가 받은 경우
* 축약(Abridged): 인정 국가 중 최소 한 곳 이상 허가받은 경우
* 전체(full): 상기 3가지 경우에 해당하지 않는 경우
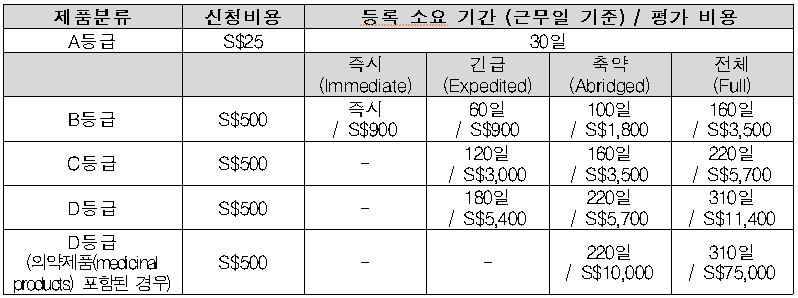
자료원: KOTRA 싱가포르 무역관 자료 종합
- 싱가포르 정부가 인정하는 국가에서의 제품 등록, 판매 경험이 없는 경우, 최대 310일의 심사시간과 총 7만5000싱가포르달러(약 6200만 원)의 비용이 소요될 수 있음.
ㅇ 태국
- 태국에 의료기기 등 제품을 수출하기 위해 태국식약청(TFDA) 등록이 필수이며, 최소 2개월에서 최대 6개월이 걸리고 과도한 서류를 요구하는 등 절차가 까다로움.
- 또한, 외국 수출업체의 경우 직접 수입허가를 신청할 수 없고, 현지 수입업자나 유통업체를 통해 제품을 등록해야 하는 등 제약이 많음.
- 태국의 의료기기는 일반의료기기(General Medical Device), 신고의료기기(Notification Medical Device), 허가의료기기(Licensing Medical Device)로 나뉠 수 있으며, TFDA의 관리 방법에 따라 지시된 사항은 아래와 같음.

자료원: 한국보건산업진흥원
ㅇ 필리핀
- 필리핀의 수입 의료기기에 대한 비관세 조치는 다른 국가보다 상대적으로 적은 편이나, 제품 등록을 하기 위해 다양한 서류를 준비해야 함.
- 필리핀에 의료기기 수출할 때 주로 제품등록증명서와 수입업자의 경우, 의료기기 영업면허가 필요함.
- 제품 등록을 위한 신청 비용은 1515페소(약 4만 원) 소요
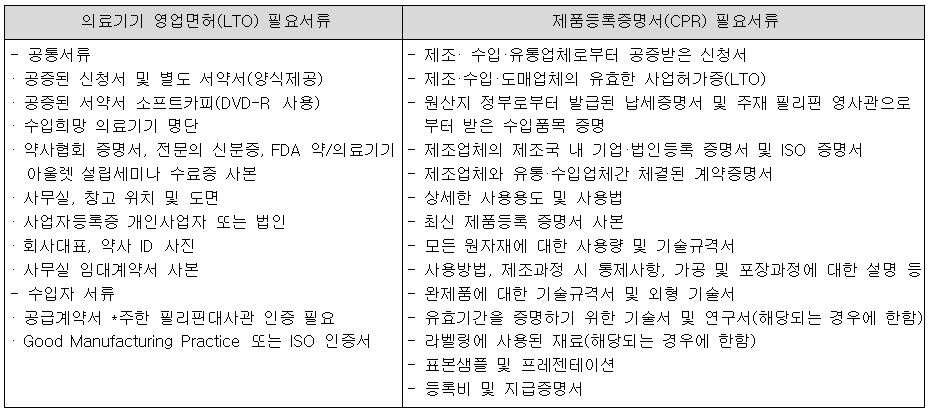
자료원: KOTRA 마닐라 무역관 자료 종합
- 필리핀에 중고 의료기기 수출도 가능하나, 환경부 검사를 필히 받아야 함.
ㅇ 인도네시아
- 인도네시아에 의료기기를 수출하려면 먼저 인도네시아 보건부에서 유통업 허가증을 취득한 후 또는 취득한 자를 통해 제품 허가증을 발급받아야 함.
- 유통업 허가증은 보건부 지방청으로부터 검사를 받은 후 받게 되는 검사보고서와 추천서를 보건부에 제출하고, 평가를 받는 두 단계에 걸친 절차를 통해 발급받을 수 있음.
- 제품 허가증의 유효기간은 기본 5년이나, 제조사로부터 발급 받은 위임장(Letter of Authorization)의 유효기간이 5년 미만일 경우 위임장의 유효기간에 따라 제품 허가증도 만료됨.
- 신규 등록은 3~4개월, 갱신이나 변경 등록은 2주 정도 소요
인도네시아 제품 허가증의 신청 절차

자료원: 한국보건산업진흥원
□ 통일된 아세안 의료기기 규정에 대한 전망
ㅇ 아세안은 2014년에 의료기기에 대한 국가 간 일원화된 규정으로 AMDD(ASEAN 의료기기 지령, the ASEAN Medical Devices Directive)를 도입함.
- AMDD는 아세안 국가에 통일된 형식의 의료기기 신청서 문안 채택, 시장에 나온 제품에 대한 감시 경보 시스템 설치, 일관된 의료기기 분류 기준 제정을 요구
ㅇ 하지만 아세안 국가들 간의 기술력, 인프라 등의 격차로 인해 현재 싱가포르와 말레이시아만 AMDD에 따라 일정한 성과를 거두는 반면, 나머지 국가들은 수행도가 아직 낮음.
ㅇ 2016년에 아세안 회원국들은 AMDD 이행을 위한 계획을 논의할 예정. AMDD가 시행되면 국가 간 무역장벽을 없애 아세안 의료기기 시장에 진입을 용이하게 하고, 아세안 국가에 제품 등록 절차가 간편해질 것으로 예상됨.
□ 시사점
ㅇ 아세안 국가들의 의료기기 수입에 대한 절차와 서류가 복잡하기 때문에, 우리 기업들이 아세안 각국 의료기기에 관한 규정을 사전에 잘 이해하고 규정에 따라 준비해야 시간과 비용을 줄일 수 있음.
ㅇ 또한, 아세안 대부분 국가의 등록 서류는 자국 언어로 작성, 혹은 수입허가를 현지 업체만 신청할 수 있는 등 규정이 있으므로 현지 에이전트를 활용하거나 현지 업체와 협력하는 것이 바람직함.
ㅇ 우리 기업들이 아세안 국가의 기술규제를 확인한 후 자사 의료기기 수출에 장벽으로 작용하거나 규제 원문에 구체적으로 명시되지 않은 사항들에 대해 한국전자정보통신산업진흥원(KEA)을 통해 TBT(무역기술장벽) 중앙사무국에 의견을 제시할 수 있음. TBT 중앙사무국은 발굴된 기업 애로에 대해 관계부처와 협력해 해소방안을 모색함.
자료원: Trademap, 한국무역협회, 한국보건산업진흥원, 국가기술표준원, EMERGO 및 KOTRA 싱가포르 무역관 자료 종합
<저작권자 : ⓒ KOTRA & KOTRA 해외시장뉴스>

KOTRA의 저작물인 (아세안 비관세장벽 ③ - 의료기기)의 경우 ‘공공누리 제4 유형: 출처표시+상업적 이용금지+변경금지’ 조건에 따라 이용할 수 있습니다. 다만, 사진, 이미지의 경우 제3자에게 저작권이 있으므로 사용할 수 없습니다.
-
1
아세안 비관세장벽 ① - 현황
싱가포르 2016.11.10
-
2
해외 수입이 급증한 필리핀 의료기기 시장
필리핀 2016.07.04
-
3
베트남 의료기기 수입: 관세 및 비관세 장벽을 중심으로
베트남 2015.11.30
-
4
태국 의료기기 수입절차에 대해 알아보자
태국 2015.10.23
-
1
중국, 한국산 폴리실리콘 덤핑 재조사 착수
중국 2016-11-23
-
2
트럼프 당선이 인도네시아 비즈니스에 미치는 영향
인도네시아 2016-11-22
-
3
EU, 한국산 경량감열지에 잠정 반덤핑관세 부과
벨기에 2016-11-22
-
4
아세안 비관세장벽 ② - 철강
싱가포르 2016-11-21
-
5
캐나다, BC주 기후변화 대응 정책 방향 및 유망 진출 분야
캐나다 2016-11-21
-
6
파키스탄, 한국산 백판지 반덤핑 조사 본격화 예상
파키스탄 2016-11-21
-
1
2023년 싱가포르 바이오헬스 산업 정보
싱가포르 2023-05-23
-
2
2021년 싱가포르 IT산업 정보
싱가포르 2021-12-01
-
3
2021년 싱가포르 관광산업 정보
싱가포르 2021-11-29
-
4
2021년 싱가포르 건설산업 정보
싱가포르 2021-11-29
-
5
2021년 싱가포르 물류산업 정보
싱가포르 2021-11-29
-
6
2021년 싱가포르 금융산업 정보
싱가포르 2021-11-23













